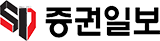오전 9시30분 경 상한가 직행
바이오기업 신라젠이 개발 중인 항암제가 국내외 임상 시험에서 유효성을 입증 받았다는 소식에 주가가 상한가를 기록했다.
27일 한국거래소에 따르면, 이날 오후 3시10분 현재 코스닥시장에서 신라젠은 가격제한폭인 29.85% 오른 5,590원을 형성해 상한가를 찍었다.
이날 전 거래일대비 6.16% 오른 4,570원에 거래를 시작한 신라젠은 상승흐름을 타다 오전 9시28분경 상한가인 5,590원으로 직행한 뒤 줄곧 이 가격을 유지하고 있다. 거래량은 417만주에 달한다.
이날 신라젠의 급등은신세포암(신장암) 환자를 대상으로 진행한 신라젠이 개발 중인 항암제 ‘펙사벡’과 미국 제약사 리제네론의 면역관문 억제제 ‘리브타요’(성분명 세미플리맙)의 병용요법이 임상 1b·2a상 시험에서 유효성과 안전성을 입증했다고 밝힌 것이 호재로 작용했기 때문이다. 펙사벡은 유전자 재조합 ‘백시니아’ 바이러스를 이용한 면역항암제 후보물질이다.
신라젠과 리제네론은 지난 2017년 11월 미국식품의약국(FDA) 임상 승인 이후 미국, 한국, 호주의 총 21개 임상기관에서 임상을 시작했다. 이후 올 초 마지막 환자의 약물 투약을 완료하고 임상을 종료했다.
해당 임상(1b·2a상)은 펙사벡과 리브타요를 함께 투여하는 병용요법의 안전성와 유효성을 확인하는 것을 목적으로 4개(A~D)의 임상군으로 구성됐다. 연구 결과 펙사벡과 리브타요를 병용으로 정맥투여한 임상군(C, D)에서 안전성 및 유효성을 입증했다고 말했다.
C군은 면역관문억제제 치료 경험이 없는 환자를 대상으로 펙사벡과 리브타요를 병용했고 23.3%의 객관적반응률(치료 반응률)과 25.1개월의 전체생존기간(OS)이 관찰됐다. 면역관문억제제 치료에 실패한 환자들을 대상으로 펙사벡과 리브타요를 병용한 D군은 17.9%의 객관적 반응률이 관측됐다.
D군은 전체 28명 중 22명이(78.6%) 이전에 세 차례 이상 약물 치료 경험이 있는 환자로 구성됐다. 5명은(17.9%) 두 차례 치료 경험이 있는 환자들이다.
통상적으로 치료경험이 많은 환자일수록 반응률이 떨어지는 것을 고려하면 이번 임상결과는 고무적이러눈게 신라젠 측의 설명이다.
신라젠 관계자는 “다양한 치료 옵션이 요구되는 전이성 또는 절제 불가능한 신세포암에서 항암바이러스와 면역항암제의 정맥 투여라는 새로운 치료방식을 제시할 수 있을 것”이라며 “이번 결과를 바탕으로 리제네론과 라이선스 아웃을 포함한 다양한 협력 방안에 대해 적극적으로 논의할 계획”이라고 말했다.