HLB 올해 첫 FDA 허가 기대감↑
미국 식품의약국(FDA)의 신약허가신청(NDA) 결과를 앞둔 HLB의 주가가 상승흐름을 타고 있다. 지난해 미국의 신약 허가가 크게 증가하고 항암제 분야가 가장 주목받은 것도 HLB 신약 허가 기대감을 키우고 있다.
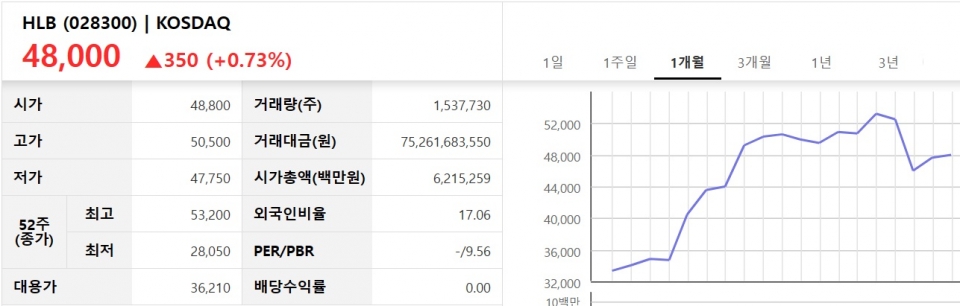
8일 한국거래소에 따르면 HLB 주가는 전 거래일 대비 0.73% 오른 48,000원에 거래를 마쳤다. 장 초반에는 50,500원까지 치솟았으나 이후 상승분을 다소 반납했다. 최근 한달간 HLB 주가는 약 50% 가량 올랐다.
1월8일 HLB 종가(왼쪽) 및 최근 한달간 HLB 주가 추이(오른쪽)
이처럼 신약 허가 기대감으로 HLB 주가가 급등한 가운데 지난해 미 FDA의 신약 허가 건수는 55건으로, 전년 대비 50% 가까이 증가한 것으로 나타났다. 한국바이오협회 바이오경제연구센터에 따르면, 지난해 미국 FDA 의약품평가연구센터(CDER)는 신물질신약(NME·합성의약품) 38개, 바이오신약(BLA) 17개, 총 55개의 신약을 허가했다. 올해는 최근 30년간 두 번째로 신약을 많이 승인한 해로 나타났다.
신약분야에서 가장 주목받는 유형은 항암제였다. 지난해 허가 받은 55건의 신약 중에서도 항암제가 13건(24%)을 차지하며, 가장 많은 수를 차지했다. 항암제는 대체적으로 시장 규모가 매우 크고 특정 암에 대해 허가를 받게 되면 다른 암에 대해서도 빠르게 적응증을 확대할 수 있다.
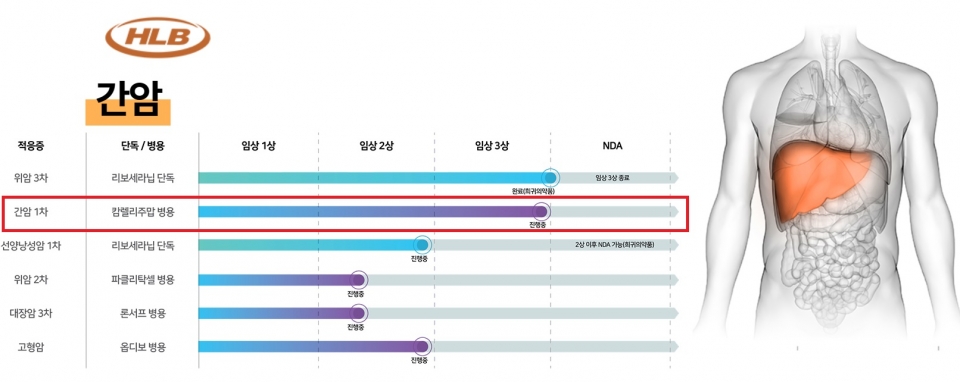
국내의 경우 올해 HLB의 간암치료제와 유한양행의 폐암치료제에 대한 기대가 크다. 특히 HLB는 리보세라닙과 캄렐리주맙을 병용요법으로 작년 5월 신약허가신청(NDA)을 완료했고, 오는 5월 내 허가여부가 결정될 예정이다.
특히 HLB는 간암시장이 가장 큰 미국에서 직접판매 전략을 실행하고 있어, 허가 시 블록버스터 매출 실현이 가능할 것이라는 전망도 나온다. 이미 미국 40개 가까운 주에서 의약품 판매 준비도 마쳤다.
이명선 DB금융투자 연구원은 “리보세라닙+캄렐리주맙에 대한 미 FDA의 단축심사(PUDFA) 일정은 올해 5월13일”이라며 “이미 FDA의 중간리뷰는 마쳤고, 현재 캄렐리주맙의 공장 실사만 남겨둔 상황”이라고 설명했다.
이어 “빠른 승인 후 미국 출시를 위해 HLB의 자회사인 엘레바는 지난해 10월 캄렐리주맙의 국내와 중국을 제외한 글로벌 판권을 간암에 한해 확보했으며, 올 상반기 미국 신약승인과는 별도로 유럽 신약승인신청도 계획하고 있다”고 덧붙였다.
금융투자업계 관계자는 “최근 국내 바이오 기업들이 굵직한 기술수출에 연이어 성공하고 있고, 세계적 학회에서도 유의미한 임상 결과를 계속 발표하며 K-바이오의 대외적 위상이 높아지고 있다”며 “HLB가 국내기업으로는 최초로 항암제 분야에서 허가를 받을 경우, HLB는 물론 높은 기술력과 성공 가능성을 가진 국내 바이오 기업을 중심으로 해외 펀드의 적극적 유입이 기대된다”고 말했다.