전일 파트너사 이뮤노반트 주가 97% 폭등
No 알부민 저해, No LDL 상승
항 FcRn 치료제 내 Best In Class 가능성
한올바이오파마(이하 한올바이오)의 미국 파트너사 이뮤노반트가 자가면역질환 치료제로 개발 중인 FcRn 항체 신약 ‘HL161ANS(IMVT-1402)’의 임상 1상 결과가 유효성 및 안정성 모두 고무적인 것으로 확인됐다. 이 같은 소식이 알려지면서 금일 한올바이오의 주가가 상한가를 기록했다.
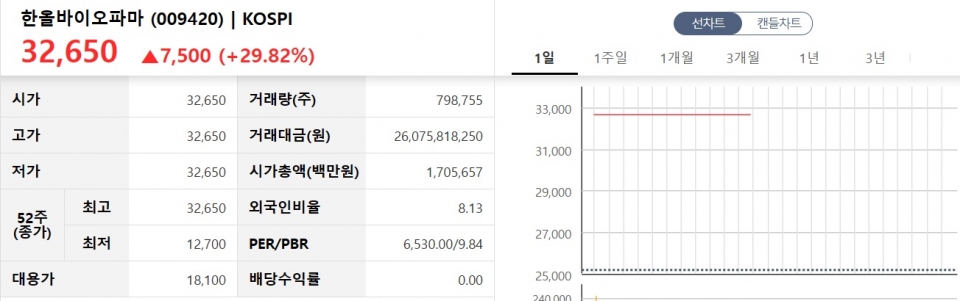
27일 한국거래소에 따르면, 이날 오전 개장 직후부터 유가증권시장에서 한올바이오파마는 전일 대비 가격제한폭(29.82%)까지 오른 32,650원에 거래되고 있다.
9월27일 한올바이오파마 주가
이러한 주가 강세는 이뮤노반트가 지난 26일(현지시간) 컨퍼런스콜에서 자가면역질환 치료제 바토클리맙(IMVT-1401)의 부작용을 보완한 후속 물질 HL161ANS(IMVT-1402)의 임상 1상 중간 데이터를 발표한 영향이다. HL161ANS는 한올바이오파마가 지난 2017년 이뮤노반트의 모회사 로이반트에 기술 이전한 FcRn 저해제 중 두 번째 항체다.
이날 발표로 이뮤노반트 주가 역시 미국 나스닥시장에서 97.04% 급등했다.
IMVT-1402 임상 1상 디자인

이뮤노반트의 발표에 따르면, 이번 1상은 건강한 참가자를 대상으로 HL161ANS 피하주사제를 두 가지 용량(300㎎, 600㎎)으로 투여하는 ‘단회용량상승시험’과 두 가지 용량을 주 1회 4주간 투여하면서 적정 용량을 평가하는 ‘다중용량상승시험’으로 구성됐다.
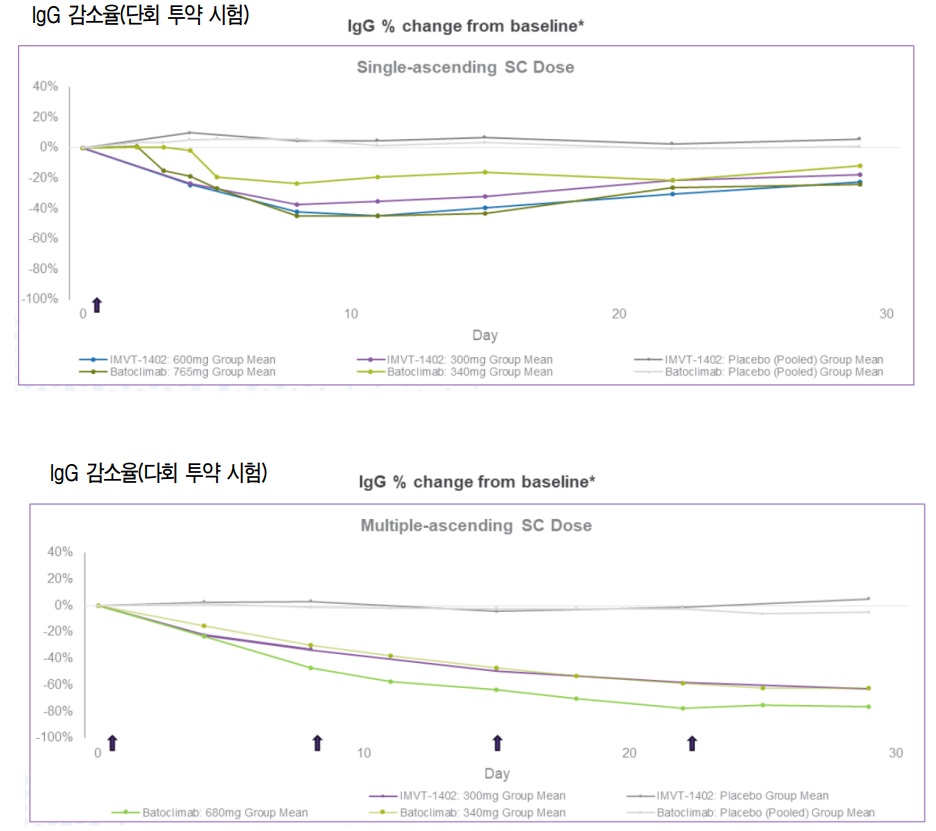
단회용량상승시험 결과 HL161ANS는 이뮤노반트의 또 다른 FcRN 항체 바토클리맙(batoclimab)과 비슷하거나 높은 수준의 항체저해 효능을 나타냈다.
안전성 측면에서는 모든 부작용이 경도 또는 중등도의 결과를 보였다. LDL-콜레스트롤 증가와 알부민 수치 감소는 모든 관찰시점에서 통계적으로 유의미한 변화가 없는 것으로 확인됐다.
4분기 공개 예정이었던 다중용량상승시험 결과 중 300㎎ 투여 데이터도 공개했다. HL161ANS 300mg을 주 1회 4주간 투약한 결과, 혈중 항체가 약 63% 감소했다. 알부민 감소나 콜레스트롤 상승은 관찰되지 않았다. 중대한 부작용도 없었다.
이뮤노반트는 최근 600㎎ 다중용량상승시험을 개시한 가운데 오는 11월 결과를 추가로 발표할 예정이다.
정승원 한올바이오파마 대표는 “하루 빨리 다음 임상 단계로 진입해 앞서 개발되고 있는 바토클리맙과 시너지를 창출하겠다”고 말했다.
김민정 DS투자증권 연구원은 “IMVT-1402 300㎎ 반복 투여 결과 약 63%에 달하는 혈중 IgG(면역글로불린G) 저해 효능을 확인했다”며 “최대용량 600㎎ 반복 투여 시 약 80% 이상 IgG 저해 효능을 보일 것으로 추정되는데 이는 항Fc리셉터(FcRn)로 달성할 수 있는 최고 수치”라고 설명했다.
지금까지 자가면역질환은 지속적인 약물투약이 필요한 경우가 많다는 점에서 바토클리맙은 적응증 확대에 한계가 있어왔다. 하지만 이번 IMVT-1402는 바토클리맙 이상의 IgG 감소 효과가 예상되는데다 혈중 알부민 영향이 없다는 점에서 다수의 자가 항체 관련 질환으로 적응증 확대가 가능할 것으로 전망된다.
또한 IMVT-1402는 SC 제형으로 개발 중인 것도 경쟁력에 유리할 것으로 판단된다. 현재 FcRn 억제제 경쟁 시장에서 SC 제형화에 성공한 약물은 비브가르트 하이트룰로(Vyvgart hytrulo)가 유일하다. 다만, 비브가르트 하이트룰로는 투약에 30~90초가 걸리는 반면 IMVT-1402는 10초 이내에 투약 완료가 가능해 편의성에서도 더 큰 장점이 될 것으로 기대된다.
하현수 유안타증권 연구원은 “IMVT-1402의 임상 1상 성공에 따른 GD 적응증 파이프라인 가치 상향과 CIDP 파이프라인 가치 추가, 성공 확률 상향 및 예상 점유율 확대가 예상된다”며 “이뮤노반트는 4분기 GD적응증의 PoC 임상결과 발표를 시작으로 내년 CIDP, MG 등 임상 결과 발표도 예정돼 있어 이에 따른 한올바이오파마의 주가는 지속 상승할 것”이라고 설명했다.